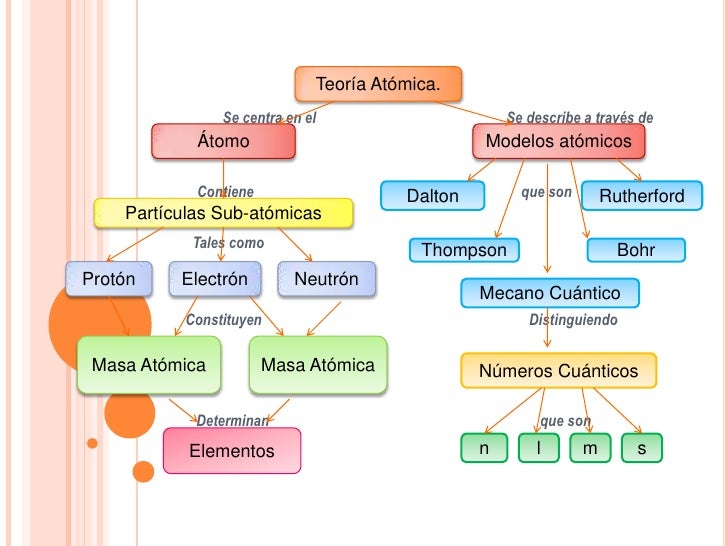
Hoy se sabe que el núcleo de cualquier átomo está constituido por protones y neutrones. A partir de ellos, se define:
Z: número atómico = nº protones del núcleo = nº electrones si el átomo está neutro.
A: número másico = nº protones + nº neutrones = partículas que hay en el núcleo.
Si dos átomos poseen el mismo número atómico Z, pertenecen al mismo elemento. Es decir, que un elemento queda perfectamente definido dando su número atómico; sin embargo, para dar más información, también se suele dar el número másico, representándose de la siguiente manera:
A: número másico = nº protones + nº neutrones = partículas que hay en el núcleo.
Si dos átomos poseen el mismo número atómico Z, pertenecen al mismo elemento. Es decir, que un elemento queda perfectamente definido dando su número atómico; sin embargo, para dar más información, también se suele dar el número másico, representándose de la siguiente manera:
 por ejemplo:
por ejemplo: 13C
 6 protones, 6 electrones y 7 neutrones
6 protones, 6 electrones y 7 neutrones 14C
 6 protones, 6 electrones y 8 neutrones
6 protones, 6 electrones y 8 neutrones 14N
 7 protones, 7 electrones y 7 neutrones
7 protones, 7 electrones y 7 neutrones con frecuencia, como vemos, el número atómico se omite, ya que al dar el símbolo del elemento queda perfectamente definido.
Concepto y tipos de isótopos
Los isótopos son átomos de un mismo elemento, (por tanto, de igual número atómico Z) con distinto número másico A, es decir, poseen diferente número de neutrones en su núcleo.
Veamos una serie de ejemplos:
- Para el carbono Z=6. Es decir, todos los átomos de carbono tienen 6 protones y 6 electrones. El carbono tiene dos isótopos: uno con A=12, con 6 neutrones y otro con número másico 13 (7 neutrones), que se representan como:


El carbono con número másico 12 es el más común (~99% de todo el carbono). Al otro isótopo se le denomina carbono-13.
- El hidrógeno presenta tres isótopos, y en este caso particular cada uno tiene un nombre diferente: hidrógeno deuterio tritio



La forma más común es el hidrógeno, que es el único átomo que no tiene neutrones en su núcleo.
Concepto y tipos de iones
Lo más habitual es que los átomos sean neutros; sin embargo, en algunas ocasiones pueden adquirir carga eléctrica. A un átomo con carga eléctrica se le llama ión. Existen 2 tipos de iones:
- Catión: es un átomo que tiene carga eléctrica positiva, lo cual significa que ha perdido uno o varios electrones de su capa más externa.
- Anión: es un átomo que tiene carga eléctrica negativa, lo cual significa que ha ganado uno o varios electrones procedentes de otro átomo y los ha incorporado a su capa más externa. La carga eléctrica de un átomo se indica mediante un superíndice (número seguido de un signo + ó -) en la parte superior derecha del símbolo del elemento químico. Ejemplos:
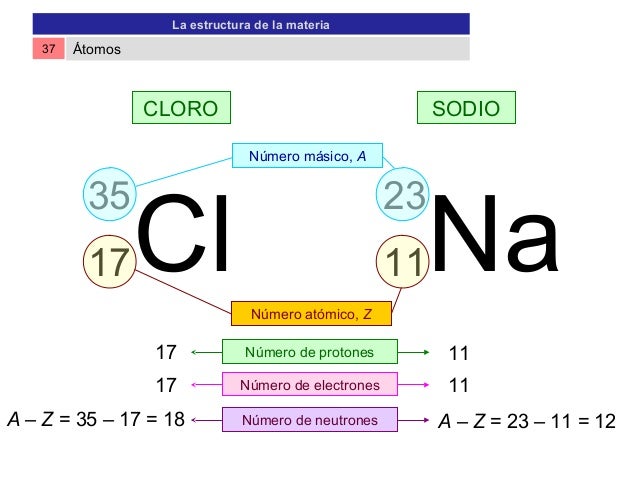
-Se trata de un átomo de cloro ; contiene 17 protones, 18 neutrones y 17 electrones. El anión CL- tendrá una carga eléctrica negativa (anión) y tendrá 18 electrones
Animaciones
Videos
A continuación os dejo una serie de videos sobre lo tratado en la unidad, los primeros tratan del número atómico y el número másico.
Finalmente os dejo un par de esquemas muy interesantes